Сера — вещество, в настоящий момент изученное человечеством практически полностью. В древности оно считалось мистическим, было окружено тайнами, легендами и мифами, которые возникали из-за суеверного страха людей перед всем неизведанным. Впрочем, многие физические свойства серы были известны людям еще до того, как Менделеев поместил элемент в периодическую таблицу и присвоил ему номер 16. Это вещество достаточно широко применялось еще в эпоху Гомера, кроме того, некоторую информацию (условно достоверную) о нем можно найти в Новом и Ветхом Заветах.

Содержание
- 1 Химический элемент
- 2 История использования
- 3 В природе
- 4 Название
- 5 Физические свойства серы
- 6 Химические свойства
- 7 Электронная структура
- 8 Месторождения
- 9 Способы добычи
- 10 Применение
- 11 Что такое сера и как она выглядит
- 12 Характеристика серы
- 13 Области применения
- 14 Нахождение серы в природе
- 15 Биологическая роль серы
- 16 СТРУКТУРА
- 17 СВОЙСТВА
- 18 МОРФОЛОГИЯ
- 19 ПРОИСХОЖДЕНИЕ
- 20 ПРИМЕНЕНИЕ
Химический элемент
В одночасье систематизировать накопленную веками информацию о таком веществе, как сера, было достаточно сложно. Этим занимались многие ученые, но определить ее принадлежность к классу химических элементов удалось Д. И. Менделееву. В периодической системе она обозначена номером 16. Расположена сера в третьем периоде, шестой группе главной подгруппы, атомная масса — 32, плотность (при нормальных условиях) — 2070 кг/м 3 .
История использования
Древние люди активно применяли физические свойства серы, которые были им известны. Источником ее возникновения считались боги земли, или подземные люди, наделенные особыми качествами. Характерный запах данного вещества и легкость его воспламенения пригодились служителями церкви при проведении различных религиозных обрядов и изгнании «злых духов». В дальнейшем сера стала применяться в военных целях, входила в состав горючих смесей. С большой долей вероятности можно утверждать, что она использовалась при создании «греческого огня», который наводил священный ужас на противника. В быту сера и ее соединения применялись в косметологии, сельском хозяйстве, с ее помощью отбеливали ткани и выводили паразитов. В древнем Китае первые пиротехнические опыты производились при помощи серы. Полученные смеси еще не являлись порохом, но послужили базой для создания его формулы, которая, к слову, в современных условиях была модернизирована. Однако на начальном этапе ее основу составляла именно сера. Химия, точнее, алхимия того времени, называет данный элемент «отцом всех металлов». Подобный вывод основывается на присутствии серы во многих рудах и ее повышенной горючести. Развеять этот миф удается Лавуазье в 1789 году. Ученый отнес элемент к неметаллам и, как показали дальнейшие исследования, был прав. В медицине соединения серы применялись в качестве антисептических и антипаразитарных средств.

В природе
В горных породах земной коры сера встречается достаточно часто. По степени доступности и распространенности она занимает 16 место среди всех химических элементов. Строение атома серы дает возможность данному веществу находиться в чистом виде (в определенных природных условиях). Но в большинстве случаев она входит в состав различных руд, в соединениях образует сульфиды и сульфаты. Наиболее распространены ее связи с металлами: железный колчедан (пирит), киноварь, свинцовый блеск (галенит), цинковая обманка (сфалерит). В Мировом океане присутствуют сульфаты магния, кальция, натрия. На сегодняшний день определено более 200 наименований минералов. Второй — по массовой доле содержания — группой являются гипс, кизерит, глауберова соль. Сера входит в состав белковых молекул, т. е. содержится в организмах животных. Очень широко представлены органические соединения: нефть, газы и природный уголь. Основным источником образования серы и ее производных являются извержения вулканов, но деятельность человека (производственная, хозяйственная) ускорила и обогатила этот процесс. Значительное количество данного вещества накоплено в подземных водах, глинах, гипсе, на дне озер и морей, в нефти, природном газе и угле, в солончаках и в водах океанов. Круговорот серы в биосфере происходит при помощи микроорганизмов, способствует этому и влага, которая испаряется с поверхности огромного водного пространства, выпадает в виде осадков и со сточными потоками рек уходит обратно в моря и океаны.

Название
В период развития алхимии существовало несколько названий, которым обозначали современный химический элемент сера. Какое вещество подразумевалось под ними — не совсем ясно, возможно, речь шла о соединениях, руде или сернистом газе. В периодической системе Менделеева сера обозначена символом S (Sulfur). Данное латинское наименование не имеет ясного происхождения, вероятно, оно было заимствовано из древнегреческого языка, а перевести его можно как «горение». У термина, употребляемого в русском языке, очень древние корни. Словом «сера» обозначались неприятно пахнущие вещества, горючие смеси. Также есть версия о происхождение названия от цвета вещества: «светло-желтый», «серый», т. е. не определенный. Так называли все смолы. Второе название вещества, не применяемое в современности, – «жупел». Также несет в себе определение понятиям горючесть и дурной запах. Филологи пришли к выводу о наличии в этом слове санскритского корня «убивать», что, вероятно, связано со свойствами сернистого газа.
Физические свойства серы

В зависимости от аллотропной модификации, варьируются связи внутри элемента. Принято выделять три образуемых вида решетки (устойчивой цепочки атомов): ромбическая, пластическая, моноклинная. Цвет, физические свойства вещества сера зависят от модификации. Самыми стабильными и распространенными являются циклические соединения S8. Именно такой вид цепочки характерен для кристаллической серы — хрупкого вещества, имеющего желтоватый оттенок. Пластическая и моноклинная модификации являются нестабильными и переходят в циклическую структуру самопроизвольно через некоторое время после получения. Формула серы в данном случае содержит символ S4 или S6. При нормальных условиях (комнатная температура) устойчивым соединением является ромбическая цепочка: в процессе нагревания вещество переходит в жидкое агрегатное состояние, затем густеет. Постепенное охлаждение образует игольчатые кристаллы моноклинной серы, которые имеют темно-желтый цвет. При взаимодействии расплавленного вещества с холодной водой образуется пластическая аллотропная модификация, которая имеет структуру, подобную резине, и состоит из нескольких полимерных цепочек, имеет грязно-желтый (темный) цвет. Наиболее часто встречается описание серы как твердого желтого вещества, которое не взаимодействует с водой, оставаясь на ее поверхности. В качестве растворителя могут применяться органические соединения: скипидар, сероуглерод и т. д. Сера в качестве простого вещества в нормальных условиях имеет следующие термодинамические свойства:
- Относительная плотность – 2,070 г/см 3 .
- Теплопроводность — 300 К.
- Температура плавления — 112 о С.
- Молярная теплоемкость — 22,6 Дж.
- Температура кипения — 444 о С.
- Молярный объем — 15,5 см 3 /моль.
В процессе нагревания число атомов серы в молекуле уменьшается. При 300 о С она является достаточно активно двигающейся жидкостью, для получения паров температуру увеличивают до 450 о С. Одноатомную серу можно получить в процессе нагревания вещества до 1760 о С (S8 – S6 – S4 – S2 — S). Данное вещество является плохим проводником электрического тока и тепла, что широко используется при его применении.
Химические свойства
Сера вступает в реакцию со всеми металлами, в результате чего образуются сульфиды. В большинстве случаев для химической реакции необходим катализатор, в качестве которого выступает нагрев. При нормальных условиях (комнатная температура) соединение происходит только со ртутью. Данное свойство используется для обезвреживания ее паров, которые образуются в результате взаимодействия капель металла с кислородом. Не взаимодействует элемент с платиной, иридием, золотом. Полученные сульфиды являются пожароопасными соединениями, которые при поджигании достаточно интенсивно горят. Сера, очищенная на открытом воздухе, реагирует с кислородом. Данное соединение характеризуется процессом образования бесцветного газа (сернистого ангидрида) и горением. Обратимая реакция взаимодействия с водородом происходит при нагреве (по аналогии с углеродом и кремнием), образующиеся газы называют сероводородом, сероуглеродом. Как и все остальные элементы VI группы таблицы Менделеева, сера взаимодействует в запаянной трубке с галогенами (фтор, бром, хлор, фосфор). При комнатной температуре реакция возможна только со фтором. Хлорид серы является веществом, наиболее широко применяемым в химической промышленности. С водой и растворами кислот не взаимодействует, соединения со щелочью обратимы — они образуются при воздействии катализатора. Многие существующие кислоты и соли образованы в результате соединения (обязательным условием является температура) серы с кислородом и водородом.

Электронная структура
Строение атома серы дает возможность элементу проявлять себя в качестве окислителя и восстановителя, а при химической реакции иметь различную валентность. Это обусловлено распределением электронов по уровням. Ядро атома имеет заряд +16 при атомной массе 32 (16 протонов и нейтронов), радиус — 127 пм. Схема серы (электронная) выглядит следующим образом: S+16)2)8)6; в спокойном состоянии — 1S 2 2S 2 2P 6 3S 2 3P 4 . На третьем уровне атом серы имеет пять незанятых орбиталей, поэтому валентность в его соединениях варьируется в следующих пределах: -2, +2,+4,+6, которые зависят от степени его возбуждения.
Месторождения
Количество добываемой серы увеличивается ежегодно. Это связано с достаточно широким кругом ее применения, который постоянно растет за счет технологических прорывов и более тщательного исследования уже известных химических элементов. В природе сера содержится в самородном виде и входит в состав большого количества руд. В зависимости от этого применяются различные способы ее добычи. Стратиформные месторождения распространены в США, Ираке, среднем Поволжье и Прикарпатье. Они являются наиболее рентабельными в процентном отношении, там добывают от 50 до 60 % серы. Карбонатные и сульфатные породы пролегают огромными пластами, достигающими десятков метров в глубину и нескольких сотен — в длину. Солянокупольные месторождения характерны для регионов интенсивной добычи нефтепродуктов. К самым крупным залежам относят зону Мексиканского залива, которую параллельно разрабатывают США, Чили и Мексика. Наиболее современными, недавно сформировавшимися месторождениями являются вулканогенные залежи. Их происхождение связано с тектоническими разломами земной коры и действием вулканов. Соответственно, данные месторождения располагаются в Тихом океане. Активно осваивают данные зоны Япония и Россия. На территории Евразии более распространены залежи самородной серы, которая имеет достаточно древнее происхождение и преимущественно располагается в поверхностных слоях. Уральские горы, остров Сицилия, Поволжье, Львовская область являются освоенными месторождениями, которые разрабатываются до сегодняшнего дня. Мировая добыча серы составляет более 50 млн тонн в год, при этом 30 % — самородки, 33 % — газ и нефтепродукты, 14 % — переработка производственных выбросов, 16 % — из сульфидов, 6 % — из сульфатов.

Способы добычи
В зависимости от глубины залегания серосодержащей руды используют различные методы ее извлечения и дальнейшей переработки. Физические свойства серы на первый план, независимо от способа добычи, выводят безопасность процесса. Как правило, залежи данного вещества сопровождаются большим скоплением ядовитых газов, также не исключаются случаи самовозгорания. Поверхностные рудные слои снимаются пластами при помощи экскаваторов — этот способ наименее опасен (при соблюдении всех технологических требований). Сера очищенная получается в результате ее дальнейшей переработки на соответствующих предприятиях, куда она доставляется из карьеров. Способы очистки и обогащения разнообразны: термические, центрифугальные, фильтрационные, пароводяные, экстракционные.
Гораздо сложнее производить добычу серы, которая содержится в подземных слоях. Шахтный метод — за счет выделения сопутствующего газа — практически недоступен, поэтому достаточно успешно с 1895 года применяется метод Германа Фраша. Он наиболее продуктивен при разработке богатых месторождений и дает существенную экономию транспортных расходов и затрат на дальнейшую переработку руды, так как предполагает выход чистого вещества. Принцип установки прост: рудные слои, содержащие серу, подвергаются обработке горячей водой, которая подается по трубе. Внутри нее располагаются еще два цилиндрических обособленных сосуда, которые предназначены для подачи газа и выхода готового продукта. За счет низкой температуры плавления на поверхность под давлением выходит сера с небольшим количеством примесей.
Применение
Основным потребителем серы является химическая промышленность, которая не может существовать без кислот на основе данного элемента. Текстильные, нефтеперерабатывающие, пищевые, целлюлозные, горнодобывающие сегменты производства не могут обойтись без этого вещества. Формула серы дает возможность применять ее соединения для изготовления взрывчатки, спичек, резины, косметических средств, лекарств и т. д. В сельском хозяйстве рассматриваемое нами вещество входит в состав удобрений для почвы (повышает процент усвоенного фосфора) и ядов, которыми обрабатывают семена от различных вредителей.

Сера – важнейший элемент в современной промышленности.
Особые свойства серы (антисептические и антипаразитарные) делают её незаменимым компонентном многих лекарственных препаратов.
Что такое сера и как она выглядит
Сера – химический элемент, находящийся по 16 номером в таблице Д. И. Менделеева и обозначающийся буквой S (по первой букве латинского названия Sulphur).

Молярная масса серы равна 32, 065 г/моль, атомная масса — 32,066 а. е. м. Это вещество может быть как ярко-желтого, так и коричневого цвета.

Различают порошкообразную (молотую) и жидкую серу.
Характеристика серы
Сера – вещество с переменной степенью окисления. На внешней электронной орбитали серы находятся шесть валентных электронов, для заполнения не хватает ещё двух, поэтому в соединениях с металлами и водородом она проявляет валентность -2.

При взаимодействии с кислородом и галогенами, т. е. с элементами с большей электроотрицательностью, сера может проявлять положительную валентность, например, +4 и +6.
Физические свойства
Как простое вещество, сера образует несколько аллотропных модификаций:
- Ромбическая – то, что мы привыкли называть обычной серой. Она устойчива при обычных условиях, встречается чаще всего недалеко от действующих или потухших вулканов.
- Пластическая – представляет собой замкнутые или открытые цепочки соединяющейся между собой серы, получаемые обычно при её сжигании. Имеет самую большую молекулярную массу среди всех разновидностей серы.
- Моноклинная (S8) – соединение серы, которое в молекулярном виде представляет собой восьмиугольник с атомами серы в вершинах. Выглядит как множество цилиндров, похожих на иглы. При комнатной температуре быстро превращается в ромбическую.

Приблизительная молярная масса одной молекулы моноклинной серы – 256 г/моль. В России сера, в основном, бывает только двух товарных видов: гранулированная и комовая.
Сера – легкоплавкое вещество, температура плавления около 120 градусов. Нерастворима в воде и не намокает про соприкосновении с ней.
Не обладает электролитическими свойствами и теплопроводностью. Плотность серы — 2,070 г/см³.
Химические свойства
В соединениях с водородом образует серную (химическая формула H2SO4) со степенью окисления серы +6 и сернистую (H2SO3) со степенью окисления +4 кислоты, которые дают соответственно сульфаты и сульфиты.

В нормальных условиях реагируют с активными металлами и ртутью, образуя сульфиды:
Также образует сульфиды при нагревании с большинством неактивных металлов, кроме платины и золота:
Проявляет восстановительные свойства в реакции с кислородом при нагревании, образуя кислотный оксид:
В реакциях с водородом образует сернистый газ, летучее бесцветное вещество с неприятным запахом тухлых яиц:
Области применения
Широко применяется в медицине, обладает антисептическими и антипаразитарными свойствами, используется для дезинфекции помещений и избавления от паразитов.

В низких концентрациях способствует формированию новых клеток эпидермиса, из-за чего её часто используют для лечения воспалений. Помимо этого сера имеет слабительное действие, а при приеме внутрь оказывает отхаркивающий эффект.
Благодаря легковоспламеняемости и горючим свойствам, сера хорошо горит. Например, самое простое, где можно взять серу, это открыть полный спичечный коробок — сера входит в состав спичечной головки.

При трении головка касается шероховатой поверхности (например, наждачной бумаги), и спичка легко загорается.
Серная кислота (H2SO4) – важнейший продукт химической промышленности, используется в качестве электролита в свинцовых аккумуляторах, применяется для получения соляной, азотной, борной и других кислот.

Серная кислота является необходимым сульфирующим средством при получении многих лекарственных веществ и красок.
Сероводород (H2S) используется для выделения чистой серы, сульфитов и серной кислоты из растворов.
Оксиды серы (SO2 и SO3) находят применения в производстве серной и азотной кислот, а также используются в бытовой химии: входят в состав отбеливателей, дезинфицирующих средств.
Нахождение серы в природе

Чаще всего в природе находится самородная сера (S), однако встречаются и её соединения с другими элементами: FeS2 (сульфат железа (II), пирит), ZnS (сульфат цинка, цинковая обманка), CaSO4*2H2O (гипс), PbS (сульфат свинца, свинцовый блеск) и другие.
Биологическая роль серы
Сера содержится в живых организмах, особенно много её в белках ногтей, волос, копыт. Общая масса серы в человеческом организме составляет около 130 грамм. Также это вещество встречается в составе некоторых витаминов и гормонов.
Сера обладает уникальными химическими и физическими свойствами, благодаря чему является важнейшим компонентом промышленности и незаменима при создании лекарственных препаратов.

Чистая желтая сера
Сера — минерал из класса самородных элементов. Сера представляет собой пример хорошо выраженного энантиоморфного полиморфизма. В природе образует 2 полиморфные модификации: a-сера ромбическая и b-сера моноклинная. При атмосферном давлении и температуре 95,6°С a-сера переходит в b-серу. Сера жизненно необходима для роста растений и животных, она входит в состав живых организмов и продуктов их разложения, ее много, например, в яйцах, капусте, хрене, чесноке, горчице, луке, волосах, шерсти и т.д. Она присутствует также в углях и нефти.
Смотрите так же:
СТРУКТУРА
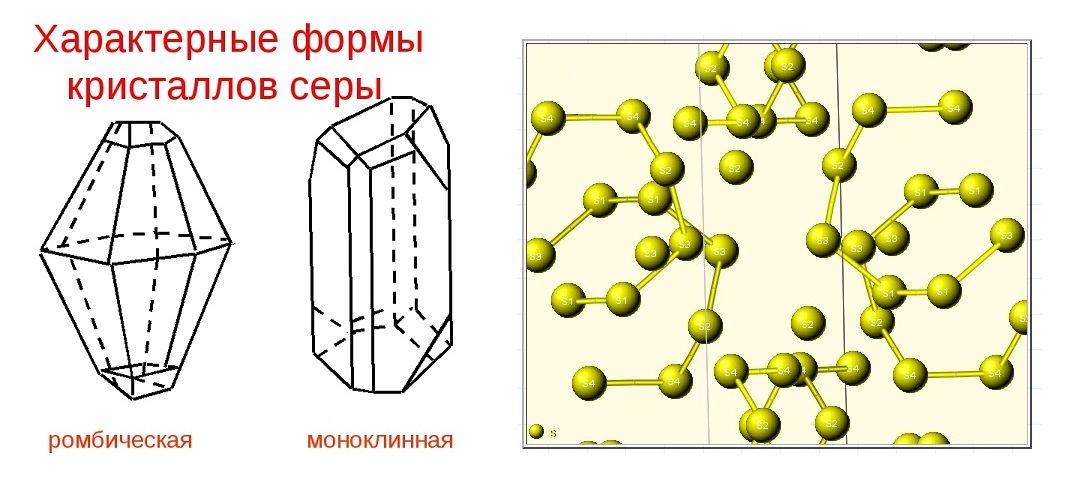
Кристаллическая структура и две сингонии серы
Самородная сера обычно представлена a-серой, которая кристаллизуется в ромбической сингонии, ромбо-дипирамидальный вид симметрии. Кристаллическая сера имеет две модификации; одну из них, ромбическую, получают из раствора серы в сероуглероде (CS2) испарением растворителя при комнатной температуре. При этом образуются ромбовидные просвечивающие кристаллы светложелтого цвета, легко растворимые в CS2. Эта модификация устойчива до 96° С, при более высокой температуре стабильна моноклинная форма. При естественном охлаждении расплавленной серы в цилиндрических тиглях вырастают крупные кристаллы ромбической модификации с искаженной формой (октаэдры, у которых частично «срезаны» углы или грани). Такой материал в промышленности называется комовая сера. Моноклинная модификация серы представляет собой длинные прозрачные темножелтые игольчатые кристаллы, также растворимые в CS2. При охлаждении моноклинной серы ниже 96° С образуется более стабильная желтая ромбическая сера.
СВОЙСТВА

Самородная сера жёлтого цвета, при наличии примесей — жёлто-коричневая, оранжевая, бурая до чёрной; содержит включения битумов, карбонатов, сульфатов, глины. Кристаллы чистой серы прозрачны или полупрозрачны, сплошные массы просвечивают в краях. Блеск смолистый до жирного. Твердость 1-2, спайности нет, излом раковистый. Плотность 2,05 -2,08 г/см 3 , хрупкая. Легко растворима в канадском бальзаме, в скипидаре и керосине. В HCl и H2SO4 нерастворима. HNO3 и царская водка окисляют серу, превращая её в H2SO4. Сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов.
Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера — хрупкое вещество жёлтого цвета. Кроме того, возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета, которая получается при резком охлаждении расплава серы (пластическая сера уже через несколько часов становится хрупкой, приобретает жёлтый цвет и постепенно превращается в ромбическую). Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами.
Плавление серы сопровождается заметным увеличением объёма (примерно 15 %). Расплавленная сера представляет собой жёлтую легкоподвижную жидкость, которая выше 160 °C превращается в очень вязкую тёмно-коричневую массу. Наибольшую вязкость расплав серы приобретает при температуре 190 °C; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °C полимерные звенья начинают рушиться.
Сера может служить простейшим примером электрета. При трении сера приобретает сильный отрицательный заряд.
МОРФОЛОГИЯ

Образует усечённо-дипирамидальные, реже дипирамидальные, пинакоидальные или толстопризматические кристаллы, а также плотные скрытокристаллические, сливные, зернистые, реже тонковолокнистые агрегаты. Главные формы на кристаллах: дипирамиды (111) и (113), призмы (011) и (101), пинакоид (001). Также сростки и друзы кристаллов, скелетные кристаллы, псевдосталактиты, порошковатые и землистые массы, налёты и примазки. Для кристаллов характерны множественные параллельные срастания.
ПРОИСХОЖДЕНИЕ

Сера образуется при вулканических извержениях, при выветривании сульфидов, при разложении гипсоносных осадочных толщ, а также в связи с деятельностью бактерий. Главные типы месторождений самородной серы — вулканогенные и экзогенные (хемогенно-осадочные). Экзогенные месторождения преобладают; они связаны с гипсо-ангидритами, которые под воздействием выделений углеводородов и сероводорода восстанавливаются и замещаются серно-кальцитовыми рудами. Такой инфильтрационно-метасоматический генезис имеют все крупнейшие месторождения. Самородная сера часто образуется (кроме крупных cкоплений) в результате окисления H2S. Геохимические процессы её образования существенно активизируются микроорганизмами (сульфатредуцирующими и тионовыми бактериями). Сопутствующие минералы — кальцит, арагонит, гипс, ангидрит, целестин, иногда битумы. Среди вулканогенных месторождений самородной серы главное значение имеют гидротермально-метасоматические (например, в Японии), образованные сероносными кварцитами и опалитами, и вулканогенно-осадочные сероносные илы кратерных озёр. Образуется также при фумарольной деятельности. Образуясь в условиях земной поверхности, самородная сера является всё же не очень устойчивой и, постепенно окисляясь, даёт начало сульфатам, гл. образом гипсу.
Используется в производстве серной кислоты (около 50% добываемого количества). В 1890 г. Герман Фраш предложил плавить серу под землёй и извлекать на поверхность через скважины, и в настоящее время месторождения серы разрабатывают главным образом путём выплавки самородной серы из пластов под землёй непосредственно в местах её залегания. Сера также в больших количествах содержится в природном газе (в виде сероводорода и сернистого ангидрида), при добыче газа она откладывается на стенках труб, выводя их из строя, поэтому её улавливают из газа как можно быстрее после добычи.
ПРИМЕНЕНИЕ

Сера входит в состав спичечной головки
Примерно половина производимой серы используется в производстве серной кислоты. Серу применяют для вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная — лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона. Сера находит применение для производства пиротехнических составов, ранее использовалась в производстве пороха, применяется для производства спичек.